发布日期:2026-02-14 09:11 点击次数:140
“慢加急性肝衰竭(ACLF)主题月评”是中国慢(加急)性肝衰竭联盟受《国际肝病》编辑部邀请,制作的ACLF相关学术月评专栏。本专栏每月以ACLF某一特定领域为主题展开,旨在普及ACLF的概念及意义、帮助读者快速了解有关领域的进展。希望本专栏对无论是需要了解相关领域热点的肝病专家及研究人员,或是需要实用知识、活跃于临床一线的医务工作者,均能有所裨益。
本期月评介绍了HBV-ACLF预后评估领域的最新研究成果。该研究首次利用高通量Olink蛋白组学技术结合机器学习算法,绘制了HBV-ACLF患者血浆炎症蛋白图谱,筛选出与90天死亡率密切相关的三个关键蛋白(IL-6、MMP10、CX3CL1),并构建了高精度的预测模型。这一发现不仅揭示了细胞因子-受体相互作用通路在ACLF进展中的核心作用,更为临床早期识别高危患者及辅助决策提供了强有力的工具。最后,对本月(2025.12.21-2026.1.22)PubMed上更新的ACLF相关重要文献进行简评。

关于作者:
中国慢(加急)性肝衰竭联盟(Chinese Acute-on-chronic liver failure Consortium,Ch-CLIF-C)是由上海交通大学附属仁济医院消化内科李海教授牵头,由全国17家三甲医院感染科/肝病中心共同参与成立的肝病科研合作团队,致力于探索慢加急性肝衰竭(ACLF)的发病机制、制定基于高循证等级的乙肝高流行区ACLF诊断标准。目前团队开展了全球已报道入组数最多的ACLF前瞻性多中心队列研究“CATCH LIFE”(Chinese AcuTe-on-CHronic LIver FailurE),包含2个大型队列(入组2600例的探索队列与入组1370例的验证队列)。
本期责任编辑

王宪波教授
医学博士,主任医师,教授,博士研究生导师。首批全国优秀中医临床人才,首都名中医,第七批全国老中医药专家学术经验传承指导老师,国家中医药管理局高水平重点专科带头人(中西医结合传染病)、中医肝病重点专科负责人,北京市重大疫情防治重点专科负责人。中国民族医药学会传染病分会会长、肝病分会副会长,中华中医药学会肝胆病分会副主任委员,中国医师协会中西医结合医师分会肝病学专家委员会副主任委员。以第一作者或通讯作者在Journal of Hepatology、Clin Gastroenterol Hepatol、Phytomedicine等杂志发表学术论文180余篇,其中SCI论文100余篇。授权发明专利11项,其中包括美国、欧洲和日本专利局授权的发明专利5项。以第一完成人获北京市科学技术三等奖、中华中医药学会科学技术一等奖、中华医学科技二等奖、华夏医学科技二等奖。
本期责任副编辑

张艺
首都医科大学附属北京地坛医院博士生,主攻终末期肝病与肝癌的临床研究。目前以第一/共一作者身份在等期刊发表SCI论文5篇。
主题述评
HBV-ACLF病情进展迅猛,短期死亡率极高。临床上,准确预测患者预后对于决定是否启动人工肝支持或进行肝移植评估至关重要。尽管目前已有MELD-Na[1]、CLIF-C ACLF[2]等评分系统,但在特异性和敏感性上仍有提升空间。血浆蛋白组成直接反映了机体的病理生理状态,特别是低丰度的炎症介质往往承载着关键的疾病信息。既往研究受限于检测手段,难以捕捉这些微量信号[3, 4]。本研究利用Olink邻近延伸分析(PEA)技术,克服了传统方法难以检测低丰度蛋白的局限,首次全面解析了HBV-ACLF患者的炎症蛋白组学特征。研究团队通过严谨的“发现-建模-验证”三阶段设计,锁定了IL-6、MMP10和CX3CL1这一“死亡风险预测铁三角”,并证实了其基于机器学习的风险评分模型在预测准确性上显著优于现有的临床评分系统,为早期识别高危患者提供了全新方案。
01 研究背景
ACLF的核心病理机制在于全身炎症反应的失控(SIRS)及随后的免疫代谢紊乱[5,6]。既往研究多关注单一或有限的炎症指标,难以涵盖疾病的病理特征[7,8]。本研究旨在利用Olink蛋白组学手段,寻找能够反映ACLF免疫病理本质的生物标志物。研究背景数据显示,非生存组患者表现出更严重的凝血功能障碍、更高的胆红素水平以及更显著的中性粒细胞浸润,这提示了“炎症风暴”与“肝脏再生失败”之间的剧烈博弈是导致死亡的关键驱动力。
02 研究设计与方法
本研究共纳入184例HBV-ACLF患者,采用多阶段设计:1)发现阶段(n=32):利用Olink平台检测96种免疫炎症相关蛋白,通过差异表达分析(DEPs)初步筛选候选分子。2)建模阶段(n=100):结合机器学习算法(XGBoost)与SHAP解释性分析,从高维数据中降维锁定核心预测蛋白。3)验证阶段(n=52):在独立队列中利用ELISA技术对候选蛋白进行定量验证,评估模型的泛化能力。此外,研究还引入了健康对照组,并对比了新模型与现有临床评分(MELD-Na、COSSH-ACLF Ⅱ、CLIF-C ACLF)的效能。
03 研究结果概述
研究通过高通量蛋白组学分析,在非生存组中鉴定出26种显著上调的蛋白,KEGG富集分析显示其主要集中于“细胞因子-细胞因子受体相互作用”通路。通过机器学习模型层层筛选,最终确定了三个具有明确病理生理意义的核心预测因子:IL-6(反映全身炎症烈度)、MMP10(提示代偿性再生失败与病理重塑)和CX3CL1(涉及免疫细胞招募)。
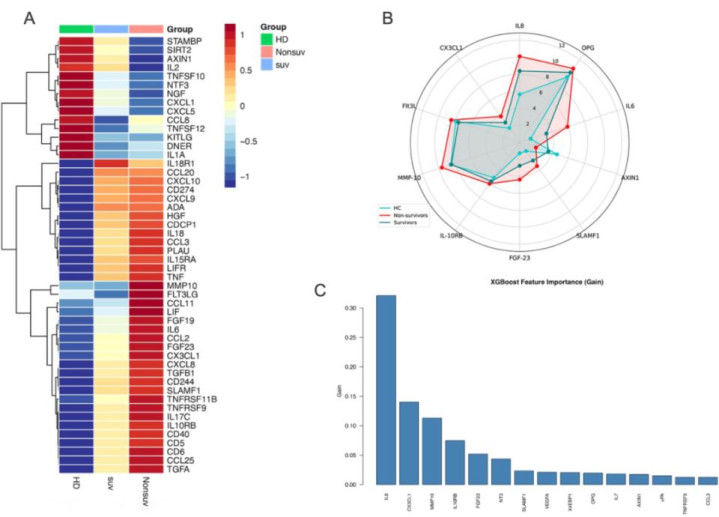
图1:候选差异蛋白的筛选与关键预测因子的鉴定。A.三组间差异蛋白表达的平均聚类热图。B.前10种差异蛋白(DEPs)相对表达量的雷达图。C. XGBoost特征重要性排序确定IL-6、CX3CL1和MMP10为首要预测因子。Zhang Y, et al. Liver Int. 2025 Dec;45(12):e70449. doi: 10.1111/liv.70449.
基于这三个蛋白构建的风险评分模型表现优异:1)预测效能高:在建模队列和独立验证队列中,预测90天死亡率的AUC分别达到0.90(95% CI:0.86-0.94)和0.87(95% CI:0.82-0.93)。2)优于传统评分:DeLong检验证实,其预测准确性显著优于MELD-Na、COSSH-ACLF II及CLIF-C ACLF等现行临床评分(P<0.05)。3)风险分层清晰:模型确定的风险截断值(0.32)能有效区分高危人群,该高危组别的90天死亡率高达75.5%~80.0%。
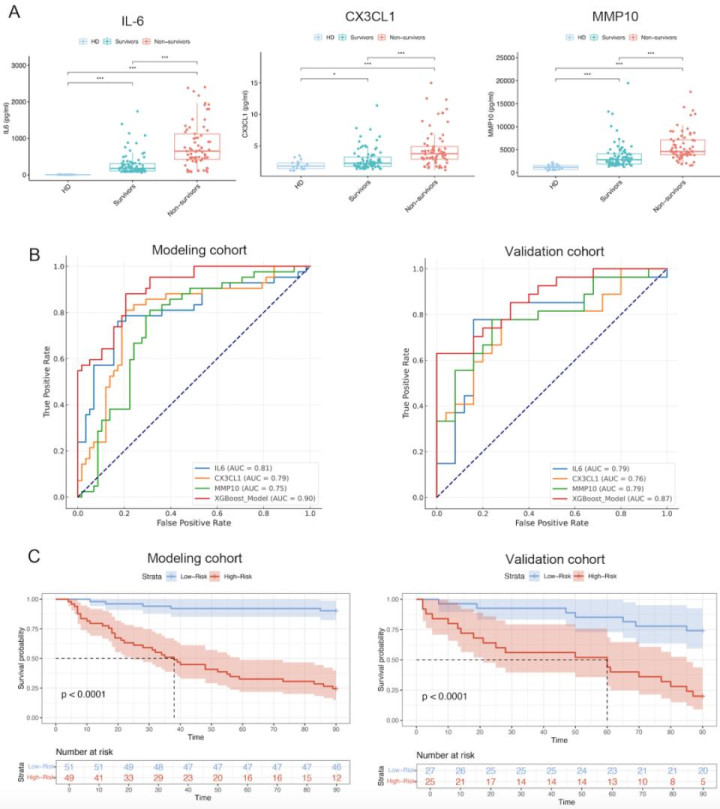
图2:关键差异蛋白(DEPs)在建模与验证队列中的验证与预测价值。A. 建模与验证队列中IL-6、CX3CL1及MMP10表达水平的ELISA验证(*P<0.05, **P<0.01, *P<0.001)。B. 建模与验证队列中,三种DEPs单独及联合预测死亡率的ROC曲线。 C. 基于IL-6、CX3CL1及MMP10复合评分的ACLF患者90天Kaplan-Meier生存曲线。Zhang Y, et al. Liver Int. 2025 Dec;45(12):e70449. doi: 10.1111/liv.70449.
04 研究意义
作为首个利用Olink技术解析HBV-ACLF炎症蛋白组学的工作,本研究不仅揭示了细胞因子受体通路异常激活在ACLF进展中的决定性作用,特别是通过MMP10的发现提出了“炎症—基质重塑—再生失败”这一导致死亡的关键病理轴,为机制研究提供了新视角。在临床转化层面,该研究提供了一个基于“IL-6 + MMP10 + CX3CL1”的高精度预后分层工具,有助于临床医生早期识别极高危患者,从而优先分配肝移植等关键医疗资源,实现精准诊疗。
总结与展望
综上所述,结合机器学习与Olink蛋白组学技术构建的预测模型,为HBV-ACLF的预后评估开辟了新路径。这项研究证明了多标志物联合模型在捕捉复杂疾病特征方面的优势。这项研究为精准医学在重症肝病中的应用奠定了基础,也提示未来的工作应致力于在多中心、跨人种的国际队列中进一步验证该模型的普适性,并深入探索针对MMP10等关键蛋白的靶向干预策略,早期精准识别高风险患者,以期改善患者预后。
参考文献:
1. Kim WR, Biggins SW, Kremers WK, Wiesner RH, Kamath PS, Benson JT, et al. Hyponatremia and mortality among patients on the liver-transplant waiting list. N Engl J Med. 2008;359(10):1018-26.
2. Jalan R, Saliba F, Pavesi M, Amoros A, Moreau R, Ginès P, et al. Development and validation of a prognostic score to predict mortality in patients with acute-on-chronic liver failure. J Hepatol. 2014;61(5):1038-47.
3. Bowser BL, Robinson RAS. Enhanced Multiplexing Technology for Proteomics. Annu Rev Anal Chem (Palo Alto Calif). 2023;16(1):379-400.
4. Haslam DE, Li J, Dillon ST, Gu X, Cao Y, Zeleznik OA, et al. Stability and reproducibility of proteomic profiles in epidemiological studies: comparing the Olink and SOMAscan platforms. Proteomics. 2022;22(13-14):e2100170.
5. Zaccherini G, Weiss E, Moreau R. Acute-on-chronic liver failure: Definitions, pathophysiology and principles of treatment. JHEP Rep. 2021;3(1):100176.
6. Br VK, Sarin SK. Acute-on-chronic liver failure: Terminology, mechanisms and management. Clin Mol Hepatol. 2023;29(3):670-89.
7. Clària J, Stauber RE, Coenraad MJ, Moreau R, Jalan R, Pavesi M, et al. Systemic inflammation in decompensated cirrhosis: Characterization and role in acute-on-chronic liver failure. Hepatology. 2016;64(4):1249-64.
8. Feio-Azevedo R, Boesch M, Radenkovic S, van Melkebeke L, Smets L, Wallays M, et al. Distinct immunometabolic signatures in circulating immune cells define disease outcome in acute-on-chronic liver failure. Hepatology. 2025;81(2):509-22.
近一月ACLF研究优秀论文简评
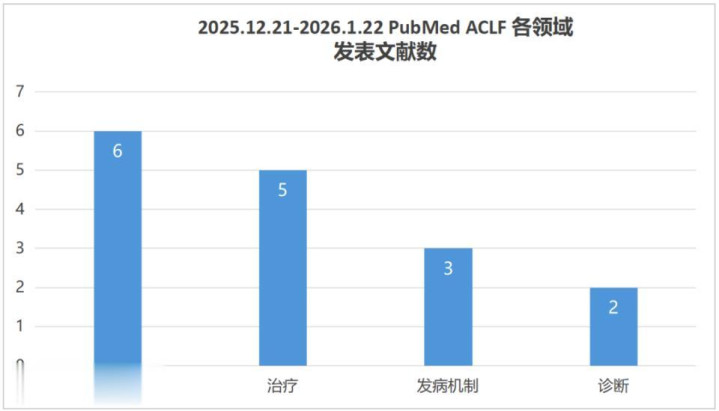
2025.12.21-2026.1.22在PubMed上在线发表ACLF相关文献共16篇,涉及疾病预测预后、治疗、诊断与发病机制,具体分布见下图。
01
Zhang M, Ji F, Zu J, et al. Unbiased clustering of acute-on-chronic liver failure patients using machine learning in a real-world ICU cohort. Nat Commun. Published online 2026. doi:10.1038/s41467-026-68368-6
简述:这项由西安交通大学、Cedars-Sinai医学中心及伦敦大学学院(Rajiv Jalan)联合发表的研究,旨在解决慢加急性肝衰竭(ACLF)定义多样且异质性高、导致风险分层困难的难题,基于MIMIC-IV重症监护数据库中1256例符合NACSELD标准的ACLF患者数据,开展了无偏机器学习聚类分析。
研究团队通过对比多种算法,最终确立了性能最优的非负矩阵分解(NMF)Lee-2模型,成功将患者划分为两个具有显著预后差异的亚型:高危组30天死亡率高达70.35%,而低危组仅为26.06%。这种风险区分能力显著优于传统基于器官衰竭数量的分级系统(I-Ⅲ级死亡率梯度为45%-69%)。
特征重要性分析意外揭示,酸碱平衡相关变量(包括碳酸氢盐、pH值、碱剩余、乳酸和阴离子间隙)是区分这两个亚型的最关键驱动因素,其权重甚至超过了传统的肝肾功能指标。该结论随后在包括失代偿期肝硬化队列、EASL-CLIF定义的ACLF队列以及外部独立队列在内的多重验证中得到了确认,证实了模型的稳健性与广泛适用性。
简评:本研究是大数据与精准医学在重症肝病领域的突破性应用。其核心创新点在于利用“无偏”的机器学习策略,跳出了传统主要依赖“器官衰竭计数”的预后评估框架,首次量化并强调了“酸碱代谢稳态”在决定ACLF患者生死中的核心地位。这一发现具有极强的临床警示意义:它提示ICU医生在救治ACLF时,应将酸碱平衡(pH、乳酸、BE)的纠正提升到与抗感染、器官支持同等的战略高度。此外,Lee-2模型展现出的“二分法”高效能,为未来识别极高危患者、制定差异化治疗方案(如紧急移植vs.姑息治疗)提供了新的理论依据。尽管模型复杂,但其揭示的病理生理规律为简化床旁评分工具指明了方向。
02
Sarin SK, Choudhury A, Kumar A, et al. Acute-on-chronic liver failure: pathophysiological mechanisms and clinical management. Nat Rev Gastroenterol Hepatol. Published online 2026. doi:10.1038/s41575-025-01159-4
简述:这篇发表在顶刊Nature Reviews Gastroenterology & Hepatology上的重磅综述,全面更新了ACLF的定义、病理生理机制、临床表现及管理策略。首先针对长期存在的定义分歧,文章介绍了“京都共识”,该共识尝试弥合亚太(APASL)与欧洲(EASL)标准的差异,通过区分以肝衰竭为主的A型和以肝外器官衰竭为主的B型,为全球诊断提供了统一标准。
在机制层面,研究深入揭示了ACLF的三重病理机制:一是免疫介导的肝细胞坏死引发炎症风暴;二是肠道微生态失调导致的细菌及毒素易位;三是免疫细胞能量代谢转向糖酵解而导致的“免疫麻痹”,这三者共同推高了多器官衰竭风险。
在管理原则上,文章界定了发病后第一周为决定预后的“黄金窗口期”,强调在此期间控制炎症和感染至关重要。在治疗上,除了器官支持和作为唯一确定性疗法的肝移植外,重点探讨了血浆置换、微生态调节及利用G-CSF或间充质干细胞促进肝再生的新兴“桥接”疗法。
简评:这篇综述是ACLF领域的“年度指南针”,其核心价值在于将ACLF的诊疗理念从单纯的“器官支持”提升到了“免疫代谢调节”与“动态精准评估”的新高度。文章强调的“动态评估”是临床管理的精髓:医生需在“黄金窗口期”内,结合MELD、AARC等评分工具每日评估病情,迅速在内科强化治疗、新兴桥接疗法或紧急移植之间做出决策。虽然“京都共识”带来了一线曙光,且再生疗法展现了潜力,但目前全球范围内肝移植资源的极度短缺(<5%获益率)依然是最大挑战。未来的突破点在于将“免疫麻痹”等机制转化为具体的药物靶点,以及通过更严格的临床试验验证非移植疗法的生存获益。
03
Dong S, Ma L, Shen C, et al. PDK4 Regulates Inflammatory Injury in Acute-on-chronic Liver Failure by Phosphorylating STAT1-mediated M1 Polarization of Macrophages. J Clin Transl Hepatol. 2025;13(12):1046-1059. doi:10.14218/JCTH.2025.00343
简述:本研究聚焦于ACLF中关键的免疫病理机制——巨噬细胞极化,旨在揭示丙酮酸脱氢酶激酶4(PDK4)在其中的调控作用。研究团队首先通过单细胞测序(scRNA-seq)和临床外周血转录组数据分析发现,ACLF患者肝脏中富集了高表达PDK4的促炎型M1巨噬细胞,且PDK4的高表达与患者28天死亡率呈正相关。随后,利用体外细胞实验和ACLF小鼠模型进行验证,结果显示:抑制PDK4能够显著阻断巨噬细胞向M1型极化,进而减少炎症介质释放,减轻对肝细胞(LO2)的毒性损伤。在分子机制层面,研究证实PDK4通过磷酸化并激活STAT1信号通路,从而驱动巨噬细胞的M1极化程序。
简评:这项研究是“免疫代谢”(Immunometabolism)理论在ACLF领域的应用。PDK4传统上被视为线粒体能量代谢的关键酶,本研究创新性地揭示了其在免疫调节中的非代谢功能,即通过“PDK4-STAT1”轴调控巨噬细胞的可塑性。这一发现具有重要的临床转化意义:它不仅解释了ACLF全身炎症反应综合征(SIRS)的部分微观机制,还提供了一个具体的药物干预靶点。即通过小分子抑制剂靶向PDK4,可能在不完全抑制免疫系统的情况下,特异性地纠正巨噬细胞的功能紊乱,从而阻断“炎症风暴”对肝脏的二次打击。未来的研究重点应放在开发高选择性的PDK4抑制剂,并在动物模型中评估其对全身能量代谢的潜在副作用。
各研究中心PI
上一篇:安集科技第三季度净利润同比增长近47% 多家机构股东减持
下一篇:没有了